Sản phẩm
PHẦN MỀM QUẢN LÝ HỆ THỐNG NƯỚC DƯỢC PHẨM
Giải pháp cho hệ thống nước tinh khiết tiêu chuẩn GMP-EU và 21 CFR Part 11:
Thiết bị RO & EDI đạt chuẩn GMP: Bao gồm màng RO chất lượng cao, hệ EDI khử ion liên tục, khung inox 316L, van vi sinh, hệ thống kiểm soát nhiệt độ & UV diệt khuẩn. Tối ưu cho nhà máy dược phẩm cần độ dẫn điện thấp, TOC dưới 500 ppb. Xem chi tiết thiết bị RO/EDI
Tủ điều khiển – SCADA – HMI cảm ứng: Lập trình trên nền PLC Siemens/Schneider kết hợp SCADA WinCC, giao diện cảm ứng 7–15" thân thiện. Ghi nhận, cảnh báo và truy xuất lô sản xuất tự động. Giải pháp tự động hoá SCADA
Phần mềm quản lý dữ liệu & báo cáo lô: Lưu trữ dữ liệu liên tục ≥2 năm, không chỉnh sửa, có chữ ký điện tử hợp chuẩn FDA. Xuất báo cáo PDF theo batch và cảnh báo sự cố từ xa.
Phần mềm quản lý hệ RO/WFI
Thiết bị RO + EDI đạt GMP
Giải pháp tự động hoá SCADA
PHẦN MỀM QUẢN LÝ HỆ THỐNG NƯỚC DƯỢC PHẨM
1. Giới thiệu
Trong ngành dược phẩm, nước tinh khiết và nước pha tiêm không chỉ là nguyên liệu sản xuất – đó là yếu tố quyết định chất lượng và an toàn của sản phẩm.
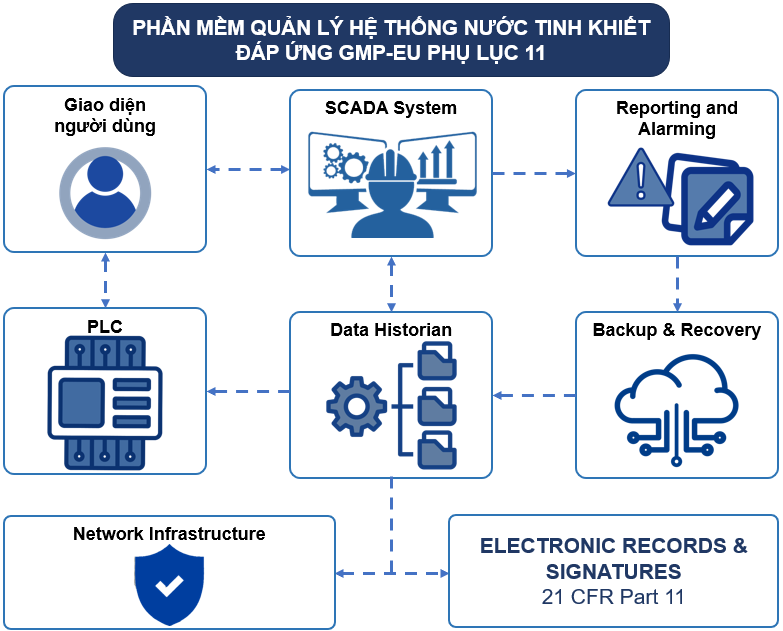
Ptech mang đến nền tảng số hóa toàn diện cho hệ thống nước dược phẩm, đáp ứng nghiêm ngặt GMP-EU Annex 11 và 21 CFR Part 11, giúp:
Giám sát & điều khiển theo thời gian thực.
Đảm bảo tính toàn vẹn dữ liệu & bảo mật.
Tích hợp linh hoạt với SCADA, BMS, DCS.
Tự động hóa báo cáo & chuẩn bị hồ sơ thẩm định.
2. Kiến trúc hệ thống phần mềm quản lý nước dược phẩm
Giao diện người dùng (UI)
Đăng nhập & phân quyền: Operator, QA, Admin.
Hiển thị trực tuyến nhiệt độ, độ dẫn điện, lưu lượng, áp suất.

Cảnh báo tức thời & xác nhận (Alarm & Acknowledgment).
Bộ điều khiển PLC
Điều khiển bơm, van, cảm biến.
Vận hành CIP/SIP, tuần hoàn, cấp nước.
Gửi dữ liệu về hệ thống SCADA.
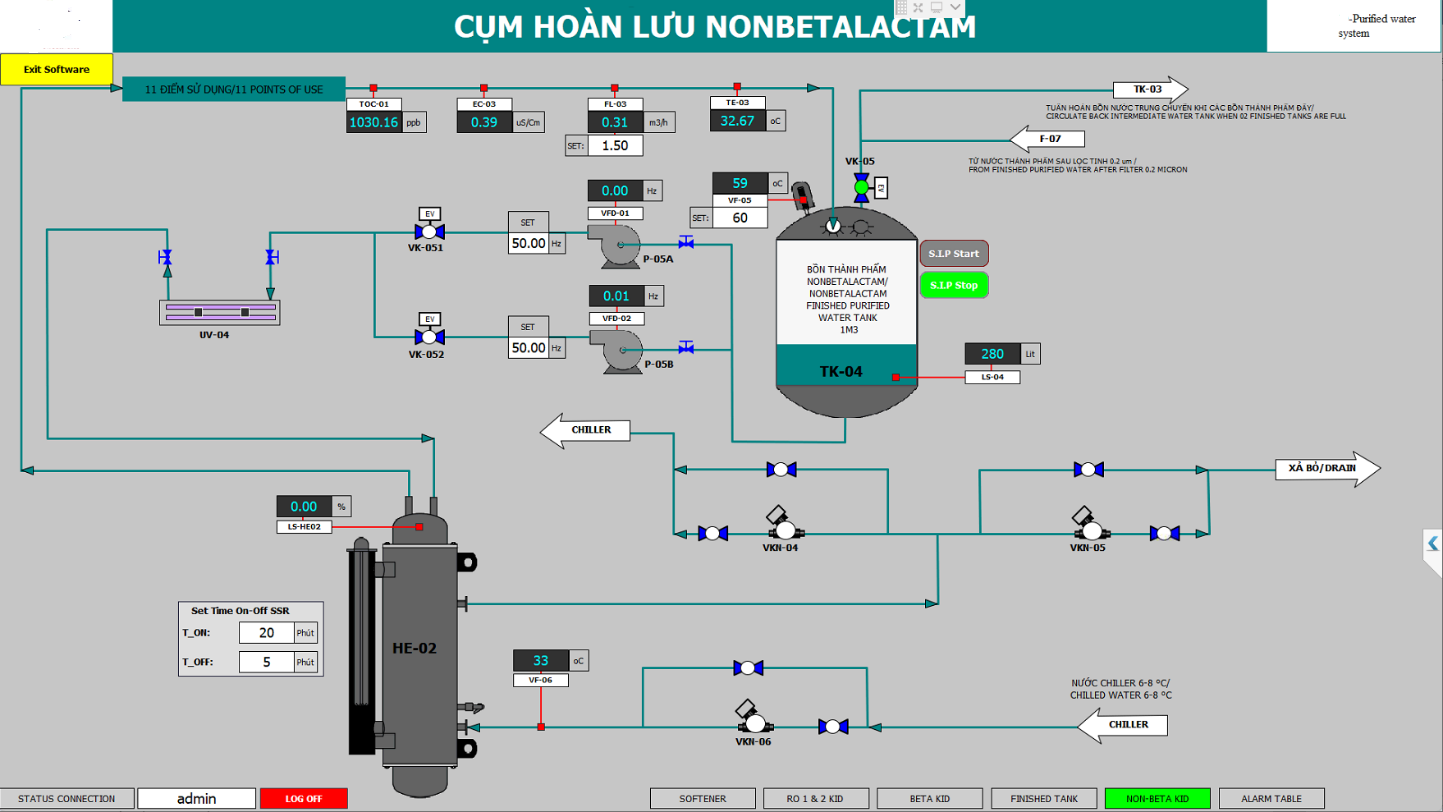
Hệ thống SCADA
Thu thập dữ liệu từ PLC.
Hiển thị quy trình trên giao diện đồ họa trực quan.
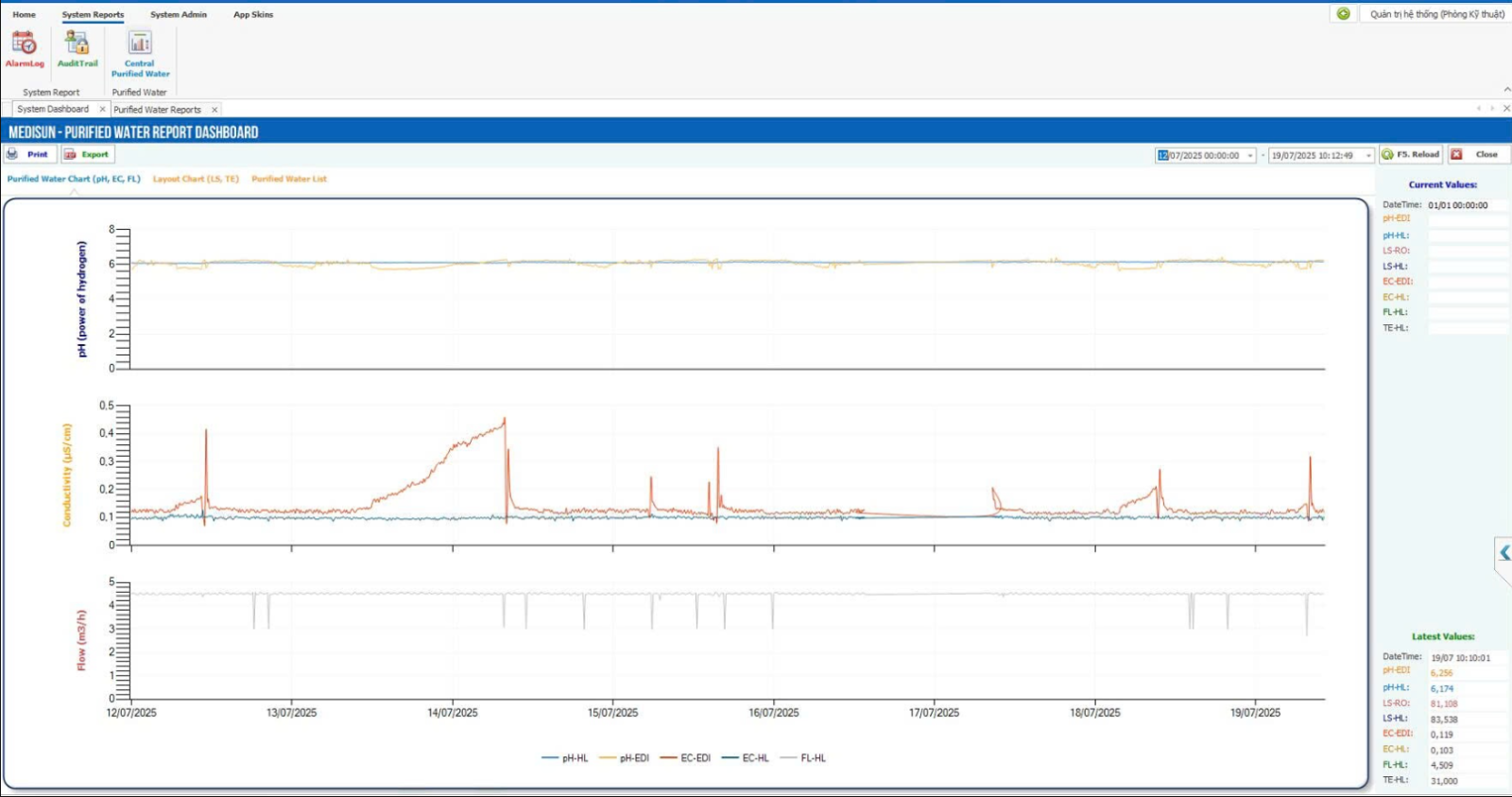
Giám sát toàn bộ hệ thống nước tinh khiết.
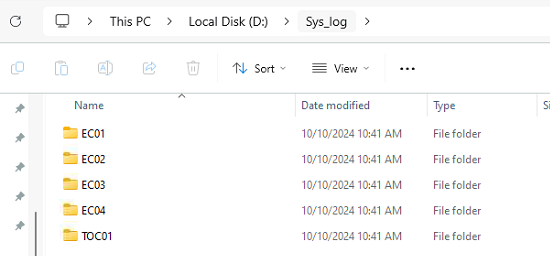
Data Historian
Ghi dữ liệu theo chu kỳ (1s, 1 phút).
Lưu trữ an toàn, không chỉnh sửa được.
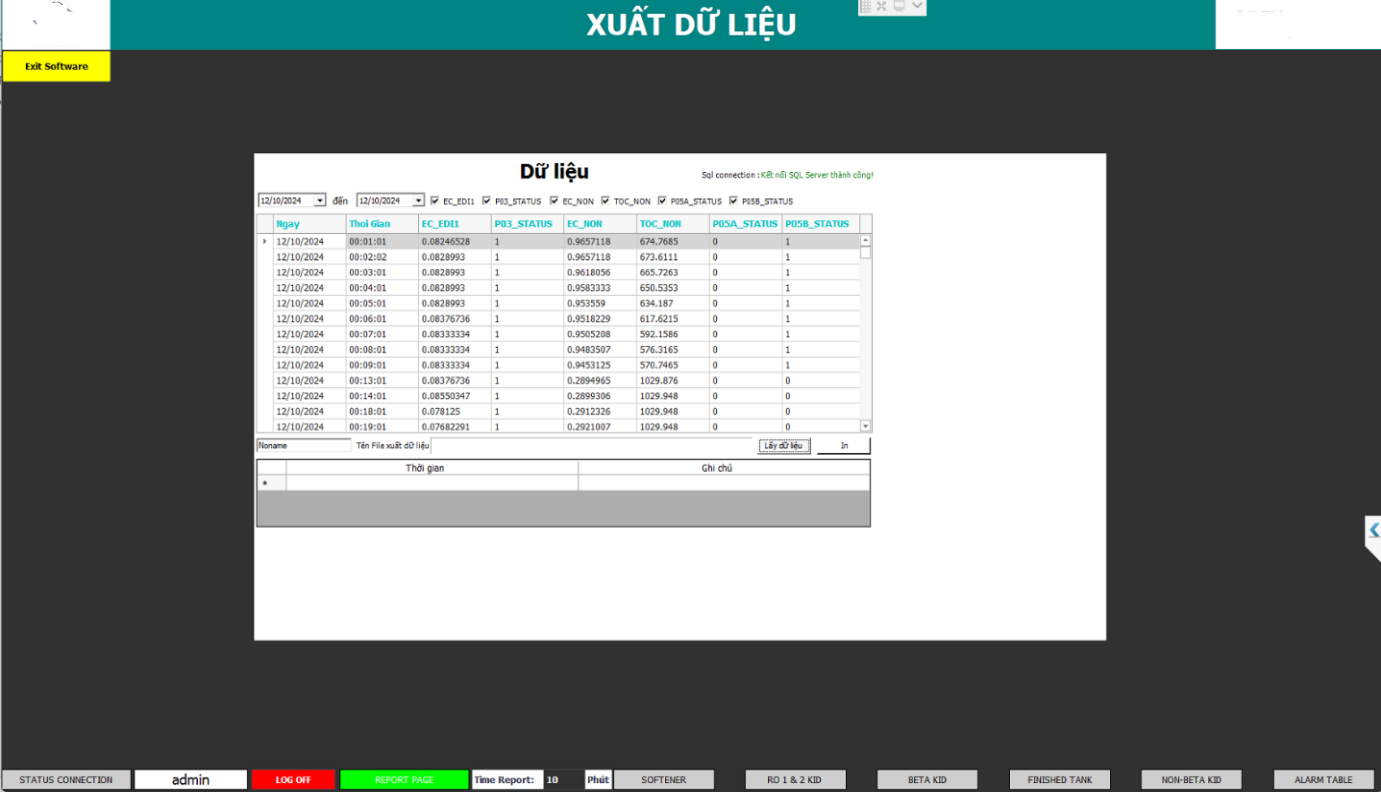
Hỗ trợ tìm kiếm & truy xuất cho QA.
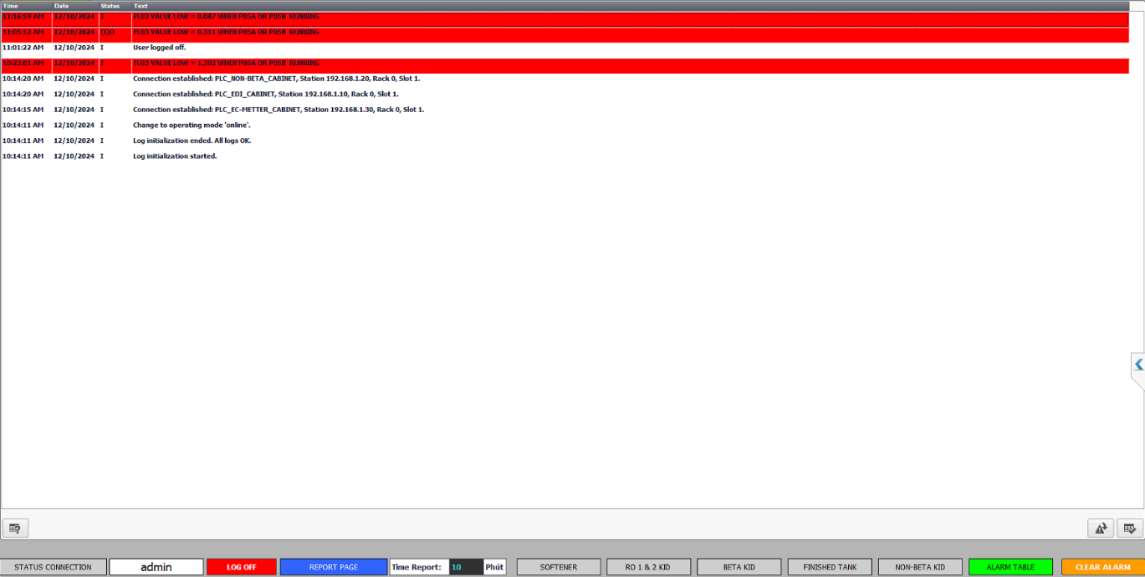
Báo cáo & Cảnh báo
Tự động tạo báo cáo hoạt động, cảnh báo, sự cố.
Xuất PDF theo từng lô sản xuất.
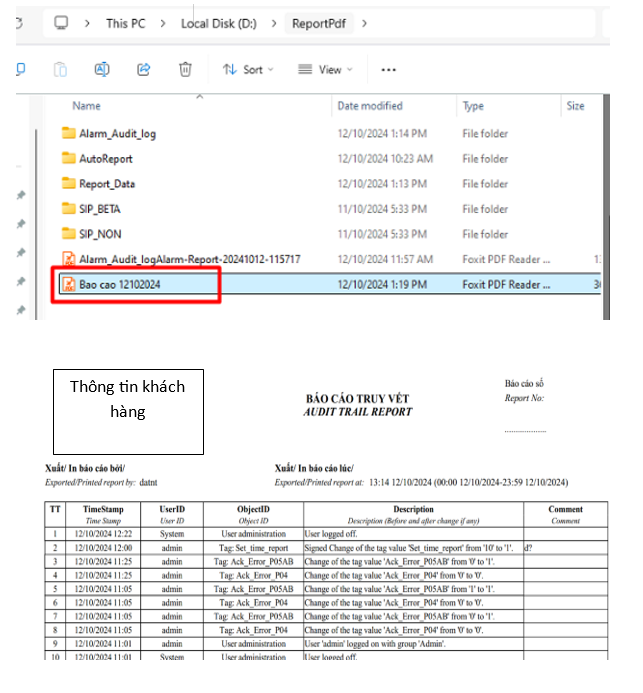
Chữ ký điện tử tuân thủ 21 CFR Part 11.
Quản lý người dùng & Audit Trail
Ghi nhật ký mọi thao tác: đăng nhập, thay đổi cấu hình, xác nhận.
Audit Trail bất biến, không xóa hoặc chỉnh sửa.
Cảnh báo hành vi không hợp lệ.
Hạ tầng mạng & Bảo mật
VPN, tường lửa, mã hóa dữ liệu.
Phân quyền truy cập chi tiết.
Bảo vệ trước các mối đe dọa mạng.
Sao lưu & Phục hồi
Lịch backup định kỳ.
Phục hồi nhanh khi sự cố.
Sao lưu ngoại tuyến (off-site).
3. Công nghệ xử lý nước tinh khiết – Đạt chuẩn GMP-WHO & USP
RO (Reverse Osmosis): Loại bỏ phần lớn khoáng & tạp chất.
Mixed Bed Ion Exchange hoặc cất nước: Hạ độ dẫn điện đến mức tiêu chuẩn dược điển.
Lọc đa tầng – Làm mềm – Than hoạt tính – UV/SUF: Loại bỏ cặn, khử mùi, bảo vệ màng RO, diệt khuẩn.
Ptech thiết kế hệ thống dựa trên nguồn nước đầu vào, tối ưu chi phí và dễ bảo trì, đảm bảo nước sau xử lý đạt Purified Water hoặc WFI theo tiêu chuẩn.
4. Tuân thủ GMP-EU Annex 11 & 21 CFR Part 11
Ptech phát triển phần mềm với các tính năng:
Quản lý người dùng & phân quyền (RBAC, mật khẩu mạnh, auto-logout).
Audit Trail đầy đủ & bất biến.
Nguyên tắc ALCOA+ đảm bảo toàn vẹn dữ liệu.
Quản lý thay đổi (Change Control) & phiên bản.
Sao lưu & phục hồi dữ liệu.
Bảo mật hệ thống (firewall, encryption).
Chữ ký điện tử hợp chuẩn.
Quản lý sự cố & báo cáo định kỳ.
5. Hồ sơ & Thẩm định hệ thống (CSV – GAMP 5)
Ptech cung cấp đầy đủ Vendor Documentation:
URS, FS, DS, SDLC, FAT, Manual, Training.
Báo cáo kiểm thử & kiểm soát phiên bản.
Hợp đồng bảo trì & hỗ trợ.
Hỗ trợ khách hàng Validation Documentation:
Risk Assessment, Test Plan, IQ, OQ, PQ.
Traceability Matrix, Validation Report.
SOP vận hành & quản trị hệ thống.
6. Yêu cầu cơ khí & chế tạo thiết bị

Thiết kế chống đọng nước, dễ bảo trì.

Mối hàn inox 316L đạt chuẩn – kiểm soát chất lượng bằng nội soi & thẩm định.


Vật tư đạt tiêu chuẩn vệ sinh, an toàn cho sản xuất dược phẩm.
7. Hỗ trơ
Với kinh nghiệm triển khai hàng chục dự án cho nhà máy dược & thực phẩm.
Giải pháp “chìa khóa trao tay”: Từ thiết kế, lắp đặt, đến thẩm định.
Hỗ trợ lâu dài: Đào tạo, bảo trì, nâng cấp phần mềm & thiết bị.
Tuân thủ tuyệt đối GMP-EU, 21 CFR Part 11, WHO, USP.
Hệ thống tương thích với các dòng PLC phổ biến như Siemens S7-1200/1500, Schneider M340/M580, Omron CP1E/NX Series, đảm bảo tính linh hoạt và dễ tích hợp cho hệ thống nước tinh khiết RO/WFI.
Chu kỳ ghi dữ liệu thời gian thực: Ghi dữ liệu với tần suất tùy chọn, phù hợp với yêu cầu giám sát liên tục trong ngành dược phẩm.
Lưu trữ dữ liệu dài hạn: Lưu trữ tùy chọn thời gian, dữ liệu không thể chỉnh sửa (đáp ứng nguyên tắc ALCOA+), truy xuất dễ dàng theo lô sản xuất hoặc ngày kiểm tra.
Hiển thị giao diện: Sử dụng Web HMI hoặc WinCC runtime, tương thích tốt với các màn hình điều khiển từ 7 đến 15 inch, thân thiện với người vận hành tại chỗ.
Giao thức truyền thông công nghiệp: Hỗ trợ Modbus TCP/IP, OPC UA, và mở rộng với MQTT, sẵn sàng kết nối với hệ thống SCADA/BMS hiện có.
Phân quyền truy cập và bảo mật: Ít nhất 03 cấp phân quyền (Operator, QA, Admin) với khả năng tích hợp xác thực 2 lớp (2FA) hoặc OTP, đảm bảo chỉ người được ủy quyền mới có thể thao tác trên hệ thống.
Chữ ký điện tử hợp chuẩn 21 CFR Part 11: Liên kết mỗi thao tác với người thực hiện, ghi nhận thời gian, lý do và xác thực danh tính, giúp hệ thống đáp ứng tiêu chuẩn FDA cho hệ thống ghi chép điện tử.
Tự động hóa báo cáo: Hệ thống tạo báo cáo tự động dưới định dạng PDF...., chia theo batch/lô sản xuất hoặc theo ngày, tuần, dễ dàng tích hợp với phần mềm ERP nội bộ.
Giải pháp sao lưu dữ liệu toàn diện: Sao lưu định kỳ theo lịch, xác minh log sao lưu thành công, hỗ trợ lưu trữ dữ liệu trên thiết bị nội bộ (NAS), USB, hoặc cloud/offsite nhằm phục hồi nhanh khi có sự cố
Tài liệu:
Installation Qualification (IQ): Xác minh rằng phần mềm và phần cứng liên quan đã được cài đặt đúng cách và phù hợp với thiết kế.
Operational Qualification (OQ): Xác minh rằng phần mềm hoạt động đúng theo các chức năng đã thiết kế trong một phạm vi hoạt động xác
định. Bao gồm kiểm tra các chức năng theo URS/FS.
Performance Qualification (PQ): Xác minh rằng hệ thống hoạt động hiệu quả và nhất quán dưới điều kiện vận hành thực tế, đáp ứng các
yêu cầu hiệu suất và chất lượng đã định.
Test Summaries / Test Reports: Báo cáo tổng hợp kết quả của các kiểm thử (IQ, OQ, PQ), ghi nhận các lỗi, sai lệch và hành động khắc phục.
Traceability Matrix (TM): Ma trận truy xuất nguồn gốc liên kết các yêu cầu của URS với các thông số thiết kế, kiểm thử và rủi ro, đảm bảo
mọi yêu cầu đều được đáp ứng và kiểm tra đầy đủ.
Validation Report (VR): Báo cáo tổng kết toàn bộ quá trình thẩm định, đưa ra kết luận về việc hệ thống có phù hợp với mục đích sử dụng và tuân thủ các quy định GxP hay không.
Standard Operating Procedures (SOPs): SOP vận hành hệ thống: Hướng dẫn sử dụng phần mềm hàng ngày. SOP quản trị hệ thống: Hướng dẫn quản lý người dùng, sao lưu, phục hồi, bảo mật.










 Nhắn tin
Nhắn tin Chỉ đường
Chỉ đường